要点
- 六方晶BaTiO3-xNyの化学組成・電子構造、触媒塩基性を解明
- 酸素空孔に捕捉された電子と隣接した窒素イオンが相互作用して、より電子密度が高く、エネルギー準位の高い窒素イオンが生成
- 超塩基に匹敵する高い塩基性と高い化学的・熱的安定性を示す
概要
東京工業大学 国際先駆研究機構 元素戦略MDX研究センターの宮﨑雅義助教、北野政明教授、細野秀雄栄誉教授らは、窒素イオンと酸素空孔が隣接した構造を有する六方晶BaTiO3-xNyが、超塩基触媒[用語1]に匹敵する高い塩基性を示すことを見出した。
炭素―炭素の結合形成やビニル基の転位反応を触媒する塩基性酸化物は、酸素原子が塩基点として作用するため、酸素イオンとの電気陰性度の差が大きいアルカリ金属やアルカリ土類金属を用いて触媒が開発されてきた。本研究では酸素イオンではなく、酸素空孔に隣接した窒素イオンを塩基点とした塩基触媒を開発した。
本研究で合成した六方晶BaTiO3-xNyは、−2価の酸素イオン(O2-)を−3価の窒素イオン(N3-)で置換するので、酸素空孔が生成し、それが窒素イオンに隣接している。酸素空孔にトラップされた電子は、隣接した窒素イオンと相互作用し、より電子密度が高く、エネルギーが高い準位を形成する。それによって、極めて高いルイス塩基性が発現する。これにより、この物質は六方晶BaTiO3-x酸化物、あるいは酸素空孔を含まない窒化物と比較して、二酸化炭素やクロロホルム吸着、クネフェナーゲル縮合反応[用語2]に対して高い触媒作用を示した。窒素イオンとそれに隣接した酸素空孔を用いた塩基触媒設計は六方晶BaTiO3系に限らず、これまで報告されている塩基触媒に対しても適用でき、普遍的な触媒設計指針を与える研究成果である。
研究成果は米国化学会誌「Journal of the American Chemical Society(ジャーナル オブ ジ アメリカン ケミカル ソサイエティー)」オンライン速報版に11月21日付で公開された。
背景
固体塩基触媒[用語3]はCO2やクロロホルム(CHCl3)といった酸性基質への電子供与により、プロトン(水素イオン、H+)引き抜きや化学結合を活性化できる物質である。水酸化ナトリウム溶液などの均一系塩基触媒と比較して、固体塩基触媒は回収・再利用が容易であり、生成物との分離が可能であるという利点を持つ。これらの触媒はオレフィンの異性化やアルコールの脱水素・脱水反応に用いられているだけでなく、メタンやアンモニアなど、これまで活性化が困難であった物質の変換反応や、CO2の変換反応に対して、塩基強度が強い固体超塩基触媒の適用が注目されている。固体塩基触媒として一般的な金属酸化物の塩基点は表面の酸素イオン(O2-)であり、高い電子密度を有する酸素原子ほど酸性基質への反応性が向上し、高い塩基性を示す。そのため、酸素と電気陰性度差が大きいアルカリ金属などを金属酸化物触媒に添加すると、塩基性が向上することが知られている。また、酸素イオンを窒素イオン(N3-)やヒドリド(H-)などのアニオン[用語4]に置き換えると電子密度が変化し、異なる塩基性を示すことが期待されるが、アニオンと塩基性の関係を明確にした報告はほとんど無い。
本研究グループは、金属酸化物触媒として六方晶BaTiO3-xHxを出発物質とすることにより、ヒドリドを窒素イオン、酸素イオン、酸素空孔に置換できることを報告している[参考文献1]。すなわち、この化合物をモデル物質とすることにより、触媒の塩基性にこれらのアニオン種が与える影響を解明できる。特に、六方晶BaTiO3-xNyは窒素イオンと酸素空孔が隣接した構造を有している。この化合物において、酸素空孔に捕捉された電子から窒素イオンへの電子供与が生じるとき、窒素イオンの電子密度が増加するだけでなく、窒素-酸素空孔電子の中間バンド[用語5]の形成によりエネルギー準位の高い窒素イオンが生成する。これにより、窒素イオンと酸性基質との反応性が向上し、より高い塩基性を示すことが期待できる。
研究成果
本研究では、合成した六方晶BaTiO3-xNyの電子状態とサイト構造を検討した。一般的に、酸素空孔に捕捉された電子は近傍に存在する金属サイトを還元する反応に消費されるが、BaTiO3-xNy中では金属サイトの還元だけでなく、窒素イオンの電子密度を増加させる。第一原理計算[用語6]から、このような窒素-酸素空孔の隣接構造により、BaTiO3-xNyはバンドギャップ間に中間バンドを有しており、窒素イオンの反応性が向上していることを明らかにした。
アニオンとしてヒドリド、酸素イオン、窒素イオンを含有するBaTiO3-xAy (A = H, O, N)の塩基強度を比較すると、BaTiO3-xNyが最も強い塩基性を示した。六方晶BaTiO3-xNyにおいて窒素イオンが塩基点として作用することは、CO2やCHCl3を強く吸着する機能によって確認された。また、窒素濃度を変更したBaTiO3-xNyを合成し、塩基強度を評価すると窒素濃度の増加と共に塩基性が向上した。第一原理計算からもBaTiO3-xNy上の窒素イオンが高い電子密度を有しており、CO2吸着サイトとして作用することが明らかになった。これらの結果は、BaTiO3-xNyの強い塩基性は表面上の窒素イオンに起因することを示唆している。

図1. 六方晶BaTiO3-xNyの表面構造とバンド構造、および酸基質との反応性
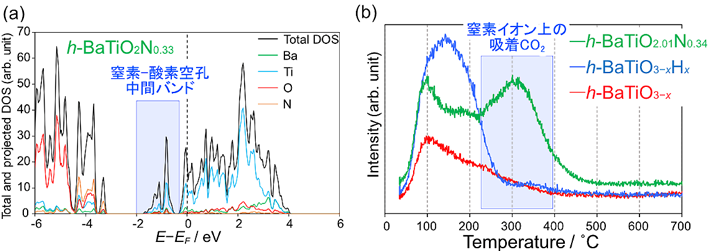
- 図2.
- (a)第一原理計算から求めたBaTiO2N0.33の密度分布
(b)ヒドリド、酸素イオン、窒素イオンを含有するBaTiO3-xAy (A = H, O, N)のCO2-TPD
触媒的な塩基性はクネフェナーゲル縮合反応を用いて評価した。クネフェナーゲル縮合はアルデヒドとニトリルの縮合反応であり、塩基触媒によってニトリルからプロトンが引き抜きされ、反応が進行する。そのため、プロトンが引き抜きにくく、酸解離定数が大きいニトリルを基質として用いたクネフェナーゲル縮合を進行させるためには、より強い塩基触媒が必要となる。本研究で合成したBaTiO3-xAy (A = H, O, N)触媒の中で、BaTiO3-xNyがクネフェナーゲル縮合に対して最も高い活性を示した。この触媒は、超塩基触媒でしか活性化できない塩基解離定数 pKa = 28.9のニトリルに対しても活性を示したことから、超塩基に匹敵する塩基触媒であるといえる。さらに、BaTiO3-xNyは大気下でも触媒活性を示し、高い再利用性を有していた。また、酸素空孔を含まない酸窒化物、および窒素イオンを含まない酸水素化物はこのような高い活性を示さなかったことから、強基性の発現のためには窒素イオンと酸素空孔が隣接した構造が必要であることが示唆された。

図3. 異なる酸解離定数(pKa)を有するニトリルを基質としたクネフェナーゲル縮合における各触媒の活性
社会的インパクト
水溶液で用いられる均一塩基触媒の塩基性は、水酸化物イオン(OH-)の塩基強度に制限され、より強い塩基性を得ることは困難である。また、液相反応での利用に限られる。一方で、固体塩基触媒は液相反応だけでなく気相反応に用いることができ、より強い塩基性を持つ触媒を用いると、これまで活性化が困難であった物質の活性化が期待できる。さらに本研究で開発した超塩基触媒は酸素イオンではなく窒素イオンが塩基点として作用するため、これまでの固体塩基触媒とは異なる性能を示す可能性がある。これらの成果は既存の塩基触媒性能の改善に留まらず、新規反応系の構築に資する結果である。
今後の展開
高い塩基性を示さないチタン酸バリウムに対して窒素イオンを導入することによって強塩基性を発現できることを明らかにした。今回の研究は固体塩基触媒において、窒素イオンと酸素空孔が塩基性に与える役割を明らかにしたものであり、今後の触媒開発に重要な指針を与える。チタン酸バリウムではなく強塩基性を示す酸化物に対しても、窒素イオンと酸素空孔を導入することにより、さらに塩基性が向上することが期待できる。
付記
今回の研究成果は、JST 創発的研究支援事業(No. JPMJFR203A)、JSPS科学研究費助成事業(No. JP20K22550、JP22H00272、JP22K18914、JP23K13600)、北海道大学触媒科学研究所共同利用・共同研究(No. 22AY0064)、JST 未来社会創造事業(No. JPMJMI21E9)、徳山財団の支援によって実施された。
用語説明
[用語1] 超塩基触媒 : 通常の塩基よりも電子供与性が強い塩基触媒であり、一般的には酸解離定数pKa = 26以上の酸性基質を活性化できる物質が超塩基触媒として定義される。
[用語2] クネフェナーゲル縮合反応 : 活性メチレン化合物とアルデヒド・ケトンの縮合反応。反応機構としては以下の段階を経てケトンが生成する。1.活性メチレン化合物のプロトン引き抜きによるカルバアニオンの形成、2.カルバアニオンのアルデヒドへの付加反応、3.付加体からの脱水反応
[用語3] 固体塩基触媒 : 塩酸や二酸化炭素、クロロホルムといった電子を受容できる酸性基質に対して、電子供与によってプロトン(H+イオン)の引き抜きや化学結合の活性化が可能な物質。
[用語4] アニオン : 負電荷を帯びたイオンの総称。1価のアニオンとして、ヒドリドイオン(H-イオン)、フッ素イオン(F-イオン)などがあり、多価のアニオンとして酸素イオン(O2-イオン)、窒素イオン(N3-イオン)などがある。
[用語5] 中間バンド : 価電子帯と伝導帯によって構築されるバンドギャップの間に形成されるエネルギーバンド。価電子帯よりも高いエネルギー準位を有しているため、中間バンドに存在している電子は価電子帯にある電子よりも高い反応性を持つ。
[用語6] 第一原理計算 : 理論計算手法の一種であり、経験的パラメーターを用いずに物質の構造や安定性、反応性を解析することができる。
参考文献
[1] M. Miyazaki, K. Ikejima, K. Ogasawara, M. Kitano, H. Hosono, Ammonia Synthesis over Fe-Supported Catalysts Mediated by Face-Sharing Nitrogen Sites in BaTiO3-xNy Oxynitride. ChemSusChem 2023, e202300551. DOI: 10.1002/cssc.202300551.
論文情報
掲載誌 : |
Journal of the American Chemical Society |
論文タイトル : |
BaTiO3–xNy: Highly Basic Oxide Catalyst Exhibiting Coupling of Electrons at Oxygen Vacancies with Substituted Nitride Ions (BaTiO3–xNy: 酸素空孔の電子と置換窒素イオンがもたらす強塩基酸化物触媒) |
著者 : |
Masayoshi Miyazaki, Hiroshi Saito, Kiya Ogasawara, Masaaki Kitano, and Hideo Hosono |
DOI : |
- プレスリリース 超塩基に匹敵する強塩基性を酸窒化物で実現 —酸素空孔に隣接する窒素イオンが塩基性反応点として機能—
- 貴金属を使わず、水に安定かつ高性能なアンモニア分解触媒を開発|東工大ニュース
- アンモニア合成を促進する新しい水素化物を開発|東工大ニュース
- 室温で二酸化炭素をメタノールへ変換できる触媒を創製|東工大ニュース
- 触媒機能をサポートする新規担体の開発に成功|東工大ニュース
- 貴金属使わずアンモニア合成触媒となる新物質発見|東工大ニュース
- 低温で高効率なアンモニア合成を実現|東工大ニュース
- 北野政明教授がアジア太平洋地域の触媒学会APACS 2022年アワードで優秀研究者賞を受賞|東工大ニュース
- 細野秀雄栄誉教授が大学発ベンチャー表彰2023で受賞|東工大ニュース
- 電子を巧みに操り、物質の潜在能力を引き出す — 細野秀雄(上)|研究ストーリー|研究
- 電子を巧みに操り、物質の潜在能力を引き出す — 細野秀雄(下)|研究ストーリー|研究
- 宮﨑雅義 Masayoshi Miyazaki|研究者検索システム 東京工業大学STARサーチ
- 北野政明 Masaaki Kitano|研究者検索システム 東京工業大学STARサーチ
- 細野秀雄 Hideo Hosono|研究者検索システム 東京工業大学STARサーチ
- 北野研究室
- 元素戦略MDX研究センター
- 国際先駆研究機構
- 物質理工学院 材料系
- 研究成果一覧
お問い合わせ先
東京工業大学 元素戦略MDX研究センター 助教
宮﨑雅義
Email miyazaki.m.ac@m.titech.ac.jp
Tel / Fax 045-924-5196
東京工業大学 元素戦略MDX研究センター 教授
北野政明
Email kitano.m.aa@m.titech.ac.jp
Tel / Fax 045-924-5191
東京工業大学 栄誉教授/同 元素戦略MDX研究センター 特命教授
細野秀雄
Email hosono@mces.titech.ac.jp
Tel / Fax 045-924-5009
取材申し込み先
東京工業大学 総務部 広報課
Email media@jim.titech.ac.jp
Tel 03-5734-2975 / Fax 03-5734-3661